发病后必死的朊病毒病迎来转机,其致死机制被破解
朊病毒(Prion),严格来说不是病毒,它们不含核酸而仅由蛋白质构成,是一类可自我复制并具感染性的小分子疏水性蛋白质,能引起哺乳动物和人的中枢神经系统病变。
人类朊病毒病是一种无法治愈的、致命的神经退行性疾病,通常表现为快速进展性痴呆。不管病因是散发性的、遗传性的还是获得性的,也不管临床名称是克雅氏病、致命性家族性失眠、或者GSS综合征,所有朊病毒病均由一个单一的分子机制导致。即都是由 PRNP 基因编码的朊病毒蛋白(PrP)的构象从其固有折叠形式(PrPC)到一种自我复制的错误折叠形式(PrPSc)的变化引起的。
关于朊病毒的研究曾两获诺贝尔生理学或医学奖,我们已经搞清楚了朊病毒的致病和传播机制,然而,朊病毒为何会导致大脑神经元死亡,却仍未完全搞清楚。
我们曾报道过两个非常有代表性的朊病毒病患者,她们代表了朊病毒病的两种患病类型。一个是 émilie Jaumain,2010年时24岁的她在实验室做绵羊适应性疯牛病小鼠模型的大脑切片,以外刺伤手指,并因此感染朊病毒。9年后,她因朊病毒感染导致的克雅氏病而去世。另一个是 Sonia Vallabh,她遗传了来自母亲的 PRNP(D178N)基因突变,该基因突变将导致朊病毒病的一种——致命性家族性失眠,该疾病通常在50岁时发病,并很快导致死亡,她目前已经37岁。
2021年12月22日,美国 Scripps 研究所的研究人员在 Science Advances 期刊发表了题为:Endosomal sorting drives the formation of axonal prion protein endoggresomes 的研究论文,该论文还被选为当期封面论文。
该研究发现,朊病毒蛋白形成的蛋白聚集体,能够进入并摧毁神经元的轴突,进而杀死神经元,导致大脑功能逐渐丧失,最终导致死亡。
其他神经退行性疾病(例如阿尔茨海默病、帕金森病)在早期也有着蛋白聚集体积累,神经元轴突肿胀等迹象,因此,这一发现的意义可能远超朊病毒疾病,可能对更常见的神经退行性疾病有着重要意义。


正常情况下,神经元能清除其胞体周围的有害蛋白,但对于轴突区域却无能为力。研究团队发现4种蛋白质——Arl8、kinesin-1、Vps41和SKIP,它们参与将朊病毒蛋白包裹、运输到神经元轴突内部,并促使朊病毒蛋白形成聚集体。研究团队进一步发现,抑制这4种蛋白质中的任何一种,朊病毒蛋白都无法进入神经元轴突。
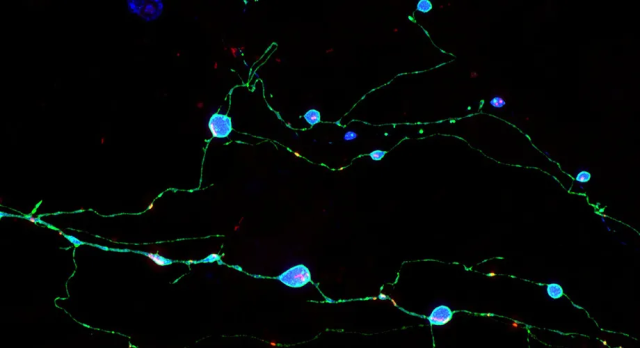
朊病毒蛋白(青色)在人类神经元轴突中富集
这一发现的意义可能远超朊病毒疾病,可能对更常见的神经退行性疾病有着重要意义。提示了我们,或许可以通过阻止有害的蛋白质进入神经元,来治疗多种神经退行性疾病。
朊病毒的发现之旅
1957年,美国科学家盖杜谢克(Daniel Gajdusek)在巴布新几内亚东部高地发现一个土著部落Fore族,Fore族有很多人得了一种被称为库鲁病的怪病,潜伏期较长,前期患者仅感头痛及关节疼痛,继之出现共济失调、震颤、不自主运动,后者包括舞蹈症、肌阵挛等,在病程晚期出现进行性加重的痴呆,神经异常。患者多在发病3~6个月内死亡。
起初,盖杜谢克以为库鲁病是遗传病,后来他发现Fore族有食用已故亲人的脏器以示怀念的习俗,盖杜谢克经过研究发现,库鲁病是一种经消化道传播的未知致病因子的传染性疾病。
在盖杜谢克的劝说下,Fore族废除了这一习俗,库鲁病从此绝迹,再未发现新的病例。盖杜谢克也因发现库鲁病这种新型的致病和传播机制,并消除了这种致命性疾病而荣获1976年的诺贝尔生理学或医学奖。库鲁病的致病源正是后来大名鼎鼎的朊病毒(Prion)。
克雅氏病是一种罕见的主要发生在50-70岁之间的可传播的脑病,受感染的人可以有睡眠紊乱,个性改变,共济失调,失语症,视觉丧失,物理,肌肉萎缩,肌阵挛,进行性痴呆等症状,并且会在发病的一年内死亡。该疾病早在1922年就被发现,但一直不清楚致病原因,也无法医治。克雅氏病是人类最常见的朊病毒病,该发病率非常低,不足百万分之一,目前全世界每年有6000多人患病。
1982年,美国生化学家史坦利·布鲁希纳(Stanley Prusiner)在 Science 发表论文,成功分离出导致克雅氏病的致病因子,并将其命名为Prion(朊病毒)。
1991年,史坦利·布鲁希纳在 Science 发表论文,揭示了朊病毒的致病机制,从而阐明了动物瘙痒症以及人类克雅氏病等致病原因。他也因此荣获了1997年的诺贝尔生理学或医学奖。
(来源:生物世界)
原文出处:Chassefeyre R, Chaiamarit T, Verhelle A, Novak SW, Andrade LR, Leit?o ADG, Manor U, Encalada SE. Endosomal sorting drives the formation of axonal prion protein endoggresomes. Sci Adv. 2021 Dec 24;7(52):eabg3693. doi: 10.1126/sciadv.abg3693. Epub 2021 Dec 22. PMID: 34936461.















