Nat Metab | 天津医科大学周洁/刘强/余鹰发现母体昼夜节律紊乱通过骨髓细胞的代谢重编程影响新生儿炎症
怀孕期间昼夜节律的破坏会对后代产生不利的健康后果;然而,母体昼夜节律在婴儿免疫系统中的作用及其对炎症的易感性仍然知之甚少。
2024年4月1日,天津医科大学周洁、刘强及余鹰共同通讯在Nature Metabolism 在线发表题为“Maternal circadian rhythm disruption affects neonatal inflammation via metabolic reprograming of myeloid cells”的研究论文,该研究证明,怀孕小鼠昼夜节律的破坏大大加重了雄性和雌性后代的新生儿炎症性疾病的严重程度,如坏死性小肠结肠炎和败血症。
母体产生二十二碳六烯酸(DHA)的减少和新生儿髓源性抑制细胞(MDSCs)的免疫抑制功能受损导致了这一现象。机制上,DHA通过PPARγ介导的线粒体氧化磷酸化增强MDSCs的免疫抑制功能。转移MDSCs或围产期补充DHA可减轻由母体节律紊乱引起的新生儿炎症。这些观察结果共同证明了母体昼夜节律在通过骨髓细胞代谢重编程控制新生儿炎症中的作用,这是以前未被认识到的。

昼夜节律是一种自我延续的振荡和对24小时周期的适应,它与外部环境信号同时同步,影响几乎所有的生理活动。昼夜节律是由转录激活因子(CLOCK/BMAL1)及其抑制因子(PERs/CRYs/REV-ERBs)组成的调节反馈回路控制的。新出现的证据已经证明了昼夜节律在免疫系统中的重要性:不同免疫细胞的细胞结构、迁移和功能都受到昼夜节律的调节。昼夜节律的破坏会导致各种免疫相关疾病。
流行病学研究和动物模型都表明,怀孕期间的次优刺激会使后代对多种疾病(包括免疫相关疾病)的易感性更高。母体昼夜节律的紊乱会导致不良的妊娠结局,如早产,甚至对成年后代的健康产生长期的恶化影响。然而,母体昼夜节律在后代免疫系统中的作用的详细机制仍然知之甚少。
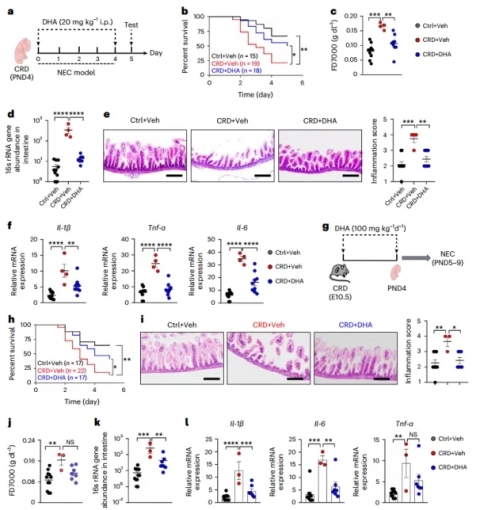
围产期补充DHA可减轻CRD模型新生儿炎症(图源自Nature Metabolism )
新生儿在出生后立即暴露于高水平的外来抗原,其中大多数是无害的,例如定植微生物群。为了避免对这些外来抗原的过度免疫激活和过度炎症,婴儿保持相对免疫耐受。婴儿期早期短暂出现的调节性免疫细胞,如MDSCs,有助于通过诱导免疫耐受来控制炎症。早产儿或低体重婴儿由于无法维持免疫耐受,患坏死性小肠结肠炎(NEC)等炎症性疾病的风险更高。母亲的昼夜节律是否会影响婴儿早期炎症性疾病的风险,这在很大程度上仍然未知。
该研究通过动物模型探讨了母体昼夜节律对新生儿炎症的潜在影响。由昼夜节律紊乱的母鼠分娩的幼崽表现出更高的NEC和败血症死亡率。母体来源DHA的减少和新生儿骨髓细胞功能受损解释了这种疾病的表型。DHA通过PPARγ介导的脂肪酸摄取和线粒体ATP生成增强新生儿髓细胞的免疫抑制功能。MDSCs的被动转移或围产期DHA补充抵消了母亲昼夜节律中断对新生儿炎症的影响。这些观察结果揭示了母体昼夜节律在新生儿炎症限制中的重要性。
(来源:iNature)
原文出处:Cui, Z., Xu, H., Wu, F. et al. Maternal circadian rhythm disruption affects neonatal inflammation via metabolic reprograming of myeloid cells. Nat Metab (2024). https://doi.org/10.1038/s42255-024-01021-y













